嬤擭丄僸僪儘僉僔僋儘儘僉儞偑偑傫帯椕偱拲栚偝傟偰偄傑偡丅
偦偺棟桼偼丄僸僪儘僉僔僋儘儘僉儞偼嵶朎撪偺僞儞僷僋幙傪暘夝偡傞僆乕僩僼傽僕乕乮autophagy乯傪慾奞偡傞嶌梡偑偁傞偨傔偱偡丅
僆乕僩僼傽僕乕慾奞栻偼偑傫帯椕栻偲偟偰奐敪偑峴傢傟偰偄傑偡偑丄僸僪儘僉僔僋儘儘僉儞偼尰帪揰偱FDA乮暷崙怘昳堛栻昳嬊乯偑彸擣偟偰偄傞堛栻昳偺拞偱僆乕僩僼傽僕慾奞嶌梡偑徹柧偝傟偰偄傞桞堦偺堛栻昳偱偡丅
僆乕僩僼傽僕乕慾奞嶌梡偼丄偑傫嵶朎偺嵶朎巰傪桿摫偟丄峈偑傫嵻姶庴惈傪崅傔傑偡丅
僆乕僩僼傽僕乕偼嵶朎撪僞儞僷僋傗彫婍姱傪擇廳偺帀幙枌偱曪傒崬傒丆偙傟傪儕僜僜乕儉偵桝憲偟暘夝偡傞堦楢偺僾儘僙僗偱偡乮壓恾乯丅
僆乕僩僼傽僕乕偺巇慻傒傪夝柧偟偨戝嬿椙揟丒搶嫗岺嬈戝塰梍嫵庼偼俀侽侾俇擭偺僲乕儀儖惗棟妛丒堛妛徿傪庴徿偟傑偟偨丅
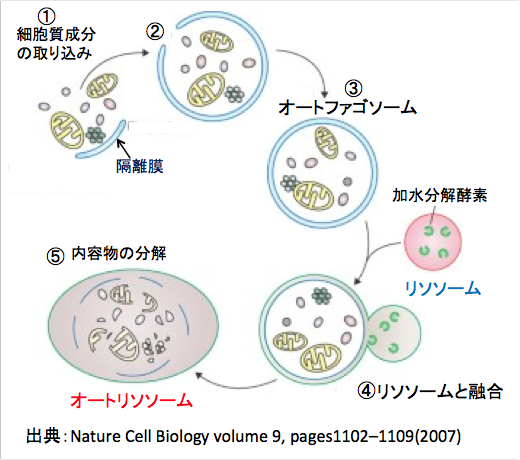
恾丗嵶朎幙偵妘棧枌偲屇偽傟傞滸暯側彫朎偑尰傟丄堎忢側僞儞僷僋幙傗嵶朎撪彫婍姱傪庢傝崬傓乮嘆乯丅偦偺屻丄枌偼嵶朎幙傪庢傝崬傒側偑傜怢挿偟乮嘇乯丄愭抂偳偆偟偑梈崌偟偰丄僆乕僩僼傽僑僜乕儉偑宍惉偝傟傞乮嘊乯丅 僆乕僩僼傽僑僜乕儉撪偵偼儈僩僐儞僪儕傾側偳偺戝偒側僆儖僈僱儔傕娷傑傟傞丅僆乕僩僼傽僑僜乕儉偑儕僜僜乕儉偲梈崌偡傞偲乮嘋乯丄撪曪暔偼暘夝偝傟傞乮嘍乯丅帺屓徚壔偱摼傜傟偨傾儈僲巁偼塰梴尮偲偟偰嵞棙梡偝傟傞丅丂丅
僆乕僩僼傽僕乕偼嵶朎撪偺堎忢僞儞僷僋幙傪暘夝偟偰儕僒僀僋儖乮嵞棙梡乯偡傞僔僗僥儉偱偡丅 峈偑傫嵻側偳偱僟儊乕僕傪庴偗偨嵶朎撪彫婍姱傗堎忢僞儞僷僋幙傪暘夝偟偰嵶朎偺僗僩儗僗晧壸乮彫朎懱僗僩儗僗乯偟丄摨帪偵塰梴屚妷偟偨忬懺偵偍偄偰丄嵶朎撪偺僞儞僷僋幙傗僄僱儖僊乕傪嶻惗偡傞偨傔偺暔幙傪摼傞偨傔偵暘夝偟偨塰梴慺傪儕僒僀僋儖偡傞偙偲偵傛偭偰惗懚傪堐帩偟傑偡丅
偟偨偑偭偰丄峈偑傫帯椕偵僆乕僩僼傽僕乕慾奞嵻傪暪梡偡傞偲丄彫朎懱僗僩儗僗偺槾恑偲丄塰梴婹夓偑槾恑偟偰嵶朎偑巰柵偟傗偡偔側偭偰丄峈偑傫嵻偺岠偒栚傪崅傔傞偙偲偑偱偒傑偡丅
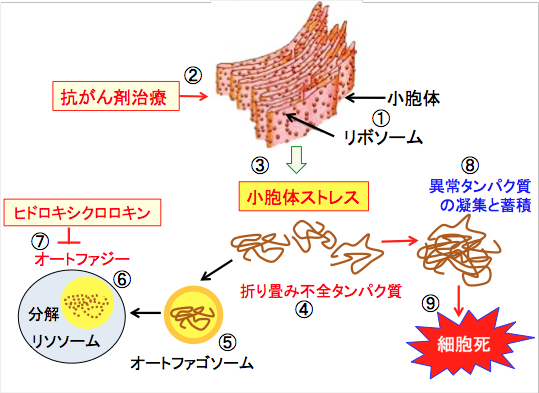
恾丗儕儃僜乕儉偱崌惉偝傟偨僞儞僷僋幙偼彫朎懱偱愜傝忯傒傗東栿岅廋忺傪庴偗偰惓忢側婡擻傪帩偭偨僞儞僷僋幙偵側傞乮嘆乯丅峈偑傫嵻帯椕偼彫朎懱偵僟儊乕僕傪梌偊乮嘇乯丄彫朎懱僗僩儗僗傪堷偒婲偙偟乮嘊乯丄彫朎懱撪偱愜忯傒晄慡偺堎忢僞儞僷僋幙偑憹偊傞乮嘋乯丅堎忢僞儞僷僋幙偼僆乕僩僼傽僑僜乕儉偵庢傝崬傑傟乮嘍乯丄儕僜僝乕儉偲桙崌偟偰僆乕僩僼傽僕乕偺儊僇僯僘儉偱暘夝偝傟丄彫朎懱僗僩儗僗傪寉尭偡傞乮嘐乯丅僸僪儘僉僔僋儘儘僉儞偼僆乕僩僼傽僕乕偺夁掱傪慾奞偡傞乮嘑乯丅偟偨偑偭偰丄峈偑傫嵻帯椕偲僸僪儘僉僔僋儘儘僉儞傪暪梡偡傞偲丄彫朎懱僗僩儗僗偑槾恑偟丄彫朎懱撪偵堎忢僞儞僷僋幙偑嬅廤偟偰拁愊偟乮嘒乯丄嵶朎婡擻偑慾奞偝傟偰嵶朎巰偑桿摫偝傟傞乮嘓乯丅



